V nedávnej americkej štúdii s adolescentami (12 – 17 rokov) hospitalizovanými kvôli SARS-CoV-2, bola počas prvých 3 mesiacov roku 2021 týždenná hospitalizácia iba 0,6 – 2,1 na 100 000 dospievajúcich detí pričom až 70 % malo súčasný výskyt viacerých ochorení. Z 31 % detí prijatých na jednotku intenzívnej starostlivosti, iba 5 % vyžadovalo mechanickú ventiláciu a nikto nezomrel. Národná štúdia z Anglicka ukázala, že vo vekovej skupine mladšej ako 18 rokov v období od marca 2020 do februára 2021 ochorenie SARS-CoV-2 spôsobilo 25 úmrtí.
Väčšina úmrtí pripadala na ázijské etnikum (36 %) a čiernu rasu (20 %). Až 60 % zomrelých dospievajúcich detí malo život obmedzujúce ochorenie a 64 % z 25 dospievajúcich detí, ktoré zomreli na SARS-CoV-2, mali ochorenia dvoch alebo viacerých telesných systémov (52 % tvorili neurologické ochorenia). Úmrtnosť adolescentov, ktorí zomreli na SARS-CoV-2, bola 0,2 na 100 000 (95 % CI 0,01 – 0,3) v porovnaní s 25,5 na 100 000 (95 % IS 24,7 – 26,5) pre všetky ostatné príčiny úmrtia, to znamená, že riziko úmrtia na SARS-CoV-2 u adolescentov bolo 127-násobne nižšie ako riziko úmrtia na iné príčiny smrti v tejto vekovej skupine.
Navyše, na rozdiel od mnohých predchádzajúcich štúdií s vážnymi metodologickými chybami, ktoré hlásili vysoký výskyt dlhého trvania infekcie SARS-CoV-2, veľa novších štúdií so zahrnutím vhodných kontrolných skupín ukázalo, že výsledky SARS-CoV-2 u detí sú podobné iným respiračným vírusovým ochoreniam a iba malá menšina hlásila pretrvávajúce symptómy po ôsmich týždňoch.
Stúpenci očkovania detí proti SARS-CoV-2 argumentujú najmä súvislosťou medzi týmto ochorením a vývinom tzv. pediatrického zápalového multisystémového syndrómu dočasne súvisiaceho so SaRS-Cov-2 (PIMS-TS)/multisystémového zápalového syndrómu u detí (MIS (-C), avšak riziko tejto zriedkavej komplikácie je extrémne nízke. Okrem toho, zvýšený výskyt tohto ochorenia u určitých etnických skupín ako sú čierna rasa, hispánska rasa a ázijské etnikum naznačuje genetickú predispozíciu k tomuto ochoreniu.
V prípade lepšej/skoršej diagnostiky ochorenia, jeho klinického priebehu a dostupnosti účinnej liečby je prognóza vyliečenia PIMS-TS/MIS (-C) veľmi priaznivá. TICMS-TS/MIS (-C) je síce závažné ochorenie so zvýšeným výskytom najmä u mužského pohlavia, dospievajúcich detí a rasových a etnických menšín, úmrtnosť je však nízka a výsledky terapie sú priaznivé.
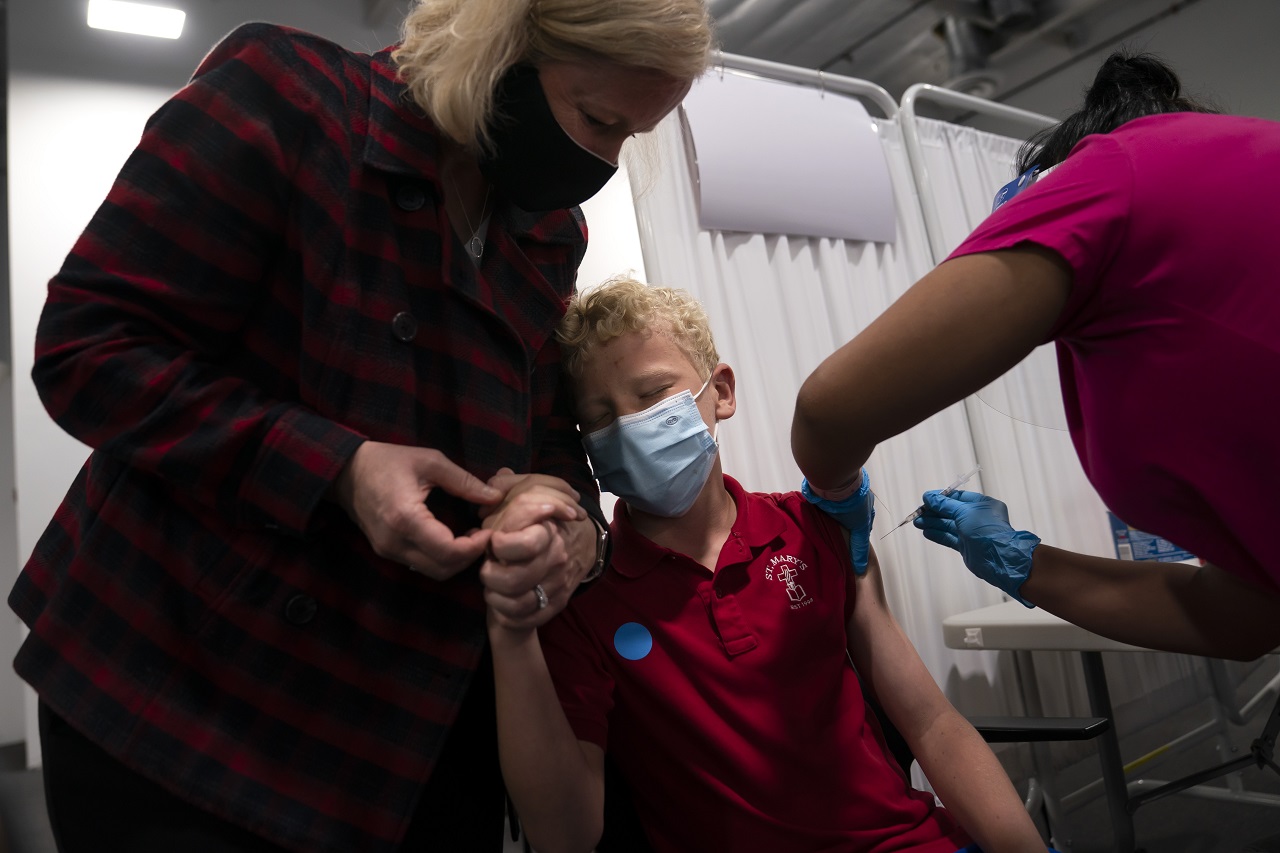
V kontraste k týmto faktom, výsledky aktuálnych štúdií jasne ukazujú, že vakcíny proti SARS-CoV-2 môžu spôsobiť u dospievajúcich detí vážne poškodenie zdravia vrátane úmrtia. Aj keď len v máji tohto roku rozšírili severoamerické, európske a ďalšie regulačné úrady možnosť núdzového použitia mRNA vakcíny (Comirnaty, Pfizer-BioNTech) pre detí vo veku 12 – 15 rokov, epidemiologické údaje o nežiaducich účinkoch vakcín proti SARS-CoV-2 rapídne pribúdajú a sú varujúce.
Americký úrad pre kontrolu potravín a liekov (FDA) vydal 23. augusta správu o vakcíne Pfizer-BioNTech, v ktorej sa poukazuje na „nadmerné riziko [myokarditídy] blížiace sa k 200 prípadom/milión,“ čo znamená, že až u 1 z 5 000 chlapcov vo veku 16 – 17 rokov sa môže vyvinúť myokarditíta po očkovaní touto vakcínou. Podľa FDA v prípade „najhoršieho scenára“ by prebytok prípadov myokarditídy/perikarditídy súvisiacej s očkovaním prevážil hospitalizáciu a úmrtia na SARS-CoV-2.
Americké CDC (Centrum pre kontrolu a prevenciu chorôb) preskúmalo svojimi lekármi 14 správ o úmrtí po očkovaní vakcínami proti SARS-CoV-2. Medzi zomrelými boli 4 dospievajúce deti vo veku 12 – 15 rokov a 10 dospievajúcich detí vo veku 16 – 17 rokov. Príčinou úmrtí boli pľúcna embólia (2 prípady), samovražda (2), intrakraniálne krvácanie (2), srdcové zlyhanie (1), hemofagocytárna lymfohistiocytóza a diseminovaná infekcia Mycobacterium chelonae (1) a neznáme alebo čakajúce ďalšie záznamy (šesť prípadov).
Štúdia v ktorej boli použité údaje zo Systému hlásenia nežiaducich udalostí týkajúcich sa vakcín (VAERS, USA), zistila významne zvýšený výskyt nežiaducich srdcových udalostí (myokarditída, perikarditída, myoperikarditída alebo bolesť na hrudníku) u dospievajúcich detí vo veku 12 – 17 rokov, a to najmä u chlapcov. Miera výskytu bola 162,2 na milión (vo veku 12 až 15 rokov) a 94 na milión (vo veku 16 až 17 rokov). Približne 86 % chlapcov z obidvoch vekových skupín bolo hospitalizovaných. U chlapcov vo veku 12 až 15 rokov, ktorí dostali druhú očkovaciu dávku mRNA vakcíny, bola miera nežiaducich srdcových udalostí 3,7 až 6,1-násobne vyššia ako ich 120-dňové riziko hospitalizácie k 21. augustu 2021 a 2,6 až 4,3-násobne vyššia v čase vysokého týždenného rizika hospitalizácie, ako napríklad v januári 2021.
V septembrovom čísle časopisu Pediatrics, bolo hlásených 7 prípadov akútnej myokarditídy alebo myoperikarditídy u chlapcov vo veku 14, 16, 16, 17,17, 18 a 19 rokov, všetci do 4 dní po druhej dávke Pfizer-BioNTech COVID-19 vakcíny. Podobne v septembrovom vydaní časopisu Journal of the American College of Cardiology Cardiovascular Imaging boli hlásené tri prípady myokarditídy u dospievajúcich chlapcov (16 – 20 rokov) 2 – 4 dní po druhej dávke Pfizer-BioNTech COVID-19.
V nedávnom reporte (august 2021) u 15 dospievajúcich detí vo veku 12 – 18 rokov hospitalizovaných pre vývin myokarditídy po očkovaní BNT162b2 (Pfizer-BioNTech) vakcínou bol klinický priebeh mierny, avšak 1 pacient mal pretrvávajúcu nízku systolickú funkciu ľavej komory, u 4 pacientov pretrvávali zmeny EKG a u jedného pacienta sa zopakovala ventrikulárna tachykardia na 6. deň, a to napriek začatiu liečby β-blokátormi.
Okrem uvedených akútnych nežiaducich účinkov vakcín proti SARS-CoV-2, ktoré sa vývinu v priebehu 1 – 2 týždňov, sú dôležité tzv. oneskorené nežiaduce účinky, ktoré sa vyvinú až po dlhšom čase od ukončenia používania lieku (napr. vývin rakoviny po liekoch, ktoré spôsobujú mutácie kovalentnou modifikáciou DNA v onkogénoch alebo tumor supresorových génoch). Výrobcovia vakcín, štát a nekritickí propagátori vakcinácie by mali 100 % garantovať, že vakcíny, ktoré obsahujú cudzí genetický materiál (mRNA kódujúcu spike proteín) a syntetické nanočastice, nemajú u detí vplyv na gény a epigenetické mechanizmy, ktoré hrajú významnú úlohu v etiológii detských chorôb vrátane rakoviny a psychických ochorení.
V Súhrne charakteristických vlastností Comirnaty sa uvádza: „Štúdie genotoxicity ani karcinogenity sa neuskutočnili. Neočakáva sa, že zložky vakcíny (lipidy a mRNA) majú genotoxický potenciál.“
Vzhľadom na fakt, že ide o očkovanie vyvíjajúcich sa detí, ktoré sú budúcnosťou národa, argumentácia „neočakáva sa“ je veľmi slabou garanciou bezpečnosti mRNA vakcíny. Zhang a kol. (máj 2021) preukázali, že RNA zo SARS-CoV-2 sa môže reverzne prepísať a integrovať do DNA kultivovaných ľudských buniek. Doerfler na základe zistenia Zhanga a kol., a na základe svojich výskumov upozorňuje, že aktuálne podávané vakcíny založené na báze vektorov adenovírusovej DNA alebo mRNA SARS-CoV-2, sa môžu reverzne prepísať do ľudskej DNA. Vakcíny na báze adenovírusového vektora môžu viesť k spojeniu ľudskej DNA s DNA adenovírusu (v prípade vakcíny AstraZeneca so šimpanzím adenovírusom) s neznámou frekvenciou a nepredvídateľnými epigenetickými dôsledkami.
Podobne SARS-CoV-2 RNA alebo jej segmenty, ako aj gén pre spike proteín sa môžu reverzne prepísať reverznými transkriptázami kódovanými LINE-1 alebo inými faktormi, a takto syntetizovaná DNA sa môže integrovať s neznámou frekvenciou a umiestnením do genómov očkovaných osôb. Podľa autora štúdie, ľudská populácia je v súčasnosti vystavená riziku integrácie cudzej DNA do ľudskej DNA v rámci obrovského experimentu, a preto by mal byť vytvorený postvakcinačný program na monitorovanie zhoršovania neočakávaných a možno aj nových ľudských chorôb u očkovaných osôb.
V žiadnom z doteraz uverejnených oficiálnych dokumentov, či už FDA (USA) alebo nášho ŠUKL (Štátny ústav pre kontrolu liečiv) sa nepíše o vplyve Comirnaty (BioNTech) na epigenetické mechanizmy (metylácia DNA, histónové modifikácie, mikroRNA a pod.), napriek tomu, že epigenetické mechanizmy regulujú tzv. bunkovú plasticitu, t. j. schopnosť bunky okamžite reagovať na vonkajšie a vnútorné podnety a zabezpečujú stabilný prenos génovej aktivity z jednej generácie buniek na ďalšie. Narušenie epigenetických mechanizmov spôsobuje vývin rôznych ochorení vrátane rakoviny, kardiovaskulárnych, respiračných a neurodegeneratívnych ochorení.
Epigenetické zmeny, ktoré sú bežné v rakovinových aj v prekanceróznych bunkách vo všeobecnosti predchádzajú mutáciám a sú ústredným prvkom vývinu nádoru pri viacerých typoch detských rakovín. Epigenetické faktory môžu s genetickými faktormi spoločne pôsobiť a podporovať vývin akútnej lymfoblastovej leukémie u detí s Downovým syndrómom. Pribúdajú dôkazy, že narušenie epigenetickej regulácie hrá významnú úlohu v etiológii porúch autistického spektra. Epigenetické mechanizmy hrajú významnú úlohu taktiež v riadení a načasovaní puberty. Narušenie epigenetických mechanizmov v sliznici maternice môže viesť k zlyhaniu implantácie ako aj k iným ochoreniam.
V kritických obdobiach embryonálneho vývinu môžu epigenetické zmeny natrvalo zmeniť epigenóm (súbor všetkých epigenetických znakov na DNA) v zárodočných bunkách, ktorý sa môže prenášať na ďalšie generácie (transgeneračná epigenetická dedičnosť).
Vakcíny proti SARS-CoV-2 by mohli ovplyvniť epigenetické mechanizmy detí jednak prostredníctvom telu cudzích nanočastíc a jednak prostredníctvom cudzej mRNA. Je známe, že lipidové nanočastice ľahko vstupujú do buniek, kde môžu priamo reagovať s genetickým materiálom alebo môžu ovplyvňovať molekuly nepriamo, čo vedie k cytotoxicite (poškodenie bunky), genotoxicite (poškodenie DNA), peroxidácii lipidov, k bunkovej smrti a dysregulácii mikroRNA (mikroRNA sú krátke nekódujúce RNA, ktoré potláčajú génovú expresiu prostredníctvom translačnej represie a/alebo degradácie cieľových mRNA).
Nanočastice môžu reagovať s mikroRNA a spôsobiť jej rozklad, alebo potlačiť transláciu (preklad genetickej informácie z poradia nukleotidov v mRNA do poradia aminokyselín v bielkovinách). Napríklad, strata funkcie mirkroRNA -259, -61/250, -42-44, -35 a -355 spôsobuje vážne funkčné poškodenia čreva, neurónov a reprodukčných orgánov. V súvislosti s rizikom, že mRNA z vakcín môže vstúpiť do interakcie s mikroRNA v ľudských bunkách je potrebné poznamenať, že interakcie mikroRNA-mRNA predstavujú významnú kontrolnú dráhu regulujúcu viaceré dôležité procesy vrátane rakoviny a embryonálneho vývinu.
Taktiež pribúdajú dôkazy, že ani polyetylénglykol (súčasť lipidových nanočastíc nesúcich mRNA) a ani syntetická mRNA kódujúca SARS-CoV-2 spike proteín nie sú voči ľudskému organizmu indiferentne, ale sú schopné vyvolať silné reakcie, vrátane život ohrozujúcich anafylaktických reakcií. Aj v súvislosti s poškodením zraku po vakcínach proti SARS-CoV-2 sa mRNA a polyetylénglykol považujú za patofyziologické príčiny tohto ochorenia. Aktuálne prebieha aspoň jedna aj keď malá štúdia (20 účastníkov) skúmajúca vplyv vakcín proti SARS-CoV-2 na epigenetické mechanizmy (methyláciu DNA) očkovaných osôb (odhadovaný dátum ukončenie štúdie je v marci 2022).
V súčasnosti je už známe a lekármi overené (CDC), že vakcína proti SARS-CoV-2 môže v priebehu pár dní či týždňov ublížiť nášmu dospievajúcemu dieťaťu alebo vyvolať nášmu dieťaťu vážne srdcovo-cievne ochorenia (akútne nežiaduce účinky). Žiaľ, zatiaľ nevieme ako ovplyvní telu cudzia mRNA a telu cudzie nanočastice obsiahnuté vo vakcínach proti SARS-Cov-2 precízne a zároveň citlivé epigenetické mechanizmy našich detí, čo sa môže prejaviť oneskorenými nežiaducimi účinkami až o pár rokov a dokonca – a to by bolo zvlášť tragické − až v nasledujúcich generáciách potomkov.
Keďže výrobcovia vakcín sa „zodpovedne“ zriekli zodpovednosti za nežiaduce účinky vakcín, preberá túto zodpovednosť na seba štát, zodpovedné orgány, zodpovední odborníci a rodičia (pokiaľ im to štát dovolí), a táto zodpovednosť sa týka nielen súčasnej, ale aj budúcich generácií potomkov. Vzhľadom na už známe riziko úmrtia dospievajúcich detí po vakcíne proti SARS-CoV-2, riziko známych akútnych nežiaducich účinkov a zatiaľ ešte nie celkom známe riziko vývinu oneskorených nežiaducich účinkov po tejto experimentálnej vakcíne, bolo by rozumné a zároveň dobré nasledovať príklad WHO, Nemecka, Švédska, Nórska a ďalších štátov, ktoré zatiaľ odložili definitívne odporúčanie očkovania pre nízkorizikové detí proti SARS-CoV-2.
PharmDr. Jozef Laurinec, PhD
Zdroje:
1. Wu Z, McGoogan JM. Characteristics of and ImportantLessonsFromtheCoronavirusDisease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72 314 CasesFromtheChinese Center forDiseaseControl and Prevention. JAMA. 2020 Apr 7;323(13):1239-1242.
2. Ladhani SN, Amin-Chowdhury Z, Davies HG, et al. COVID-19 in children: analysis of thefirstpandemicpeak in England. Archives of Disease in Childhood. 2020 Dec;105(12):1180-1185.
3. Havers FP, Whitaker M, Self JL, et al. Hospitalization of AdolescentsAged 12-17 YearswithLaboratory-Confirmed COVID-19 – COVID-NET, 14 States, March 1, 2020-April 24, 2021. MMWR MorbMortalWklyRep. 2021 Jun 11;70(23):851-857. doi: 10.15585/mmwr.mm7023e1.
4. Rando HM, Bennett TD, Byrd JB, et al. Challenges in definingLong COVID: Strikingdifferencesacrossliterature, Electronic Health Records, and patient-reportedinformation. Preprint. medRxiv. 2021;2021.03.20.21253896. Published 2021 Mar 26. doi:10.1101/2021.03.20.21253896
5. Molteni E, Sudre CH, Canas LS, et al.Illnessduration and symptom profile in a largecohort of symptomatic UK school-agedchildrentestedfor SARS-CoV-2.doi: https://doi.org/10.1101/2021.05.05.21256649.
6. Payne AB, Gilani Z, Godfred-Cato S, et al. Incidence of MultisystemInflammatorySyndrome in ChildrenAmong US PersonsInfectedWith SARS-CoV-2. JAMA NetwOpen. 2021 Jun 1;4(6):e2116420. doi: 10.1001/jamanetworkopen.2021.16420.
7. Payne AB, Gilani Z, Godfred-Cato S, et al. Incidence of MultisystemInflammatorySyndrome in ChildrenAmong US PersonsInfectedWith SARS-CoV-2. JAMA NetwOpen. 2021 Jun 1;4(6):e2116420. doi: 10.1001/jamanetworkopen.2021.16420.
8. Sood M, Sharma S, Sood I, et al. EmergingEvidence on MultisystemInflammatorySyndrome in ChildrenAssociatedwith SARS-CoV-2 Infection: a SystematicReviewwithMeta-analysis. SN Comprehensiveclinicalmedicine.2021;1-10.
9. McArdle AJ, Vito O, Patel H, et al. Treatment of MultisystemInflammatorySyndrome in Children. The New EnglandJournal of Medicine.July 2021. 385:11-22.
10. Caro-Patón GL, de Azagra-Garde AM, García-Salido A, et al. Shock and MyocardialInjury in ChildrenWithMultisystemInflammatorySyndromeAssociatedWith SARS-CoV-2 Infection: WhatWeKnow. CaseSeries and Review of theLiterature.Journal of IntensiveCareMedicine. 2021 Apr;36(4):392-403.
11. Van Heerden J, Nel J, Moodley P, et al. Multisysteminflammatorysyndrome (MIS): a multicentreretrospectivereview of adults and adolescents in South Africa. Int J InfectDis. 2021 Aug 21;111:227-232.
12. Hoste L, Van Paemel R, Haerynck F. Multisysteminflammatorysyndrome in childrenrelated to COVID-19: a systematicreview. EuropeanJournal of Pediatrics. 2021 Jul;180(7):2019-2034.
13. Frenck RW Jr, Klein NP, Kitchin N, et al. Clinical Trial Group. Safety, Immunogenicity, and Efficacy of the BNT162b2 Covid-19 Vaccine in Adolescents. The New EnglandJournal of Medicine.July2021. 15;385(3):239-250.
14. Food and DrugAdministration. SummaryBasisforRegulatoryAction (COMIRNATY). https://www.fda.gov/media/151733/download. Accessed August 27, 2021.
15. Center forDiseaeControl and Prevention. COVID-19 VaccineSafety in AdolescentsAged 12–17 Years — United States, December 14, 2020–July 16, 2021.https://www.cdc.gov/mmwr/volumes/70/wr/mm7031e1.htm. Accessed September 22, 2021.
16. Høeg TB, Krug A, Stevenson J, Mandrola J. SARS-CoV-2 mRNA vaccination-associatedmyocarditis in childrenages 12-17: a stratifiednationaldatabaseanalysis. MedRxiv2021.08.30.21262866 [Preprint]. https://www.medrxiv.org/content/10.1101/2021.08.30.21…
17. Marshall M, Ferguson ID, Lewis P, et al. SymptomaticAcuteMyocarditis in 7 AdolescentsAfter Pfizer-BioNTech COVID-19 Vaccination. Pediatrics. 2021 Sep;148(3):e2021052478.
18. Dickey JB, Albert E, Badr M, et al. A Series of PatientsWithMyocarditisFollowing SARS-CoV-2 VaccinationWith mRNA-1279 and BNT162b2. JACC CardiovascImaging. 2021;14(9):1862-1863.
19. Dionne A, Sperotto F, Chamberlain S, et al. Association of MyocarditisWith BNT162b2 Messenger RNA COVID-19 Vaccine in a CaseSeries of Children. JAMA Cardiol. 2021 Aug 10:e213471.
20. Savary C, Kim A, Lespagnol A, et al. Depictingthegeneticarchitecture of pediatriccancersthroughanintegrativegenenetworkapproach. Scientificreports. 2020 Jan 27;10(1):1224.
21. Monaco AP. Anepigenetic, transgenerational model of increasedmentalhealthdisorders in children, adolescents and youngadults. EuropeanJournal of HumanGenetics : EJHG. 2021 Mar;29(3):387-395.
22. Comirnaty: EPAR-ProductInformation. Last updated:02/06/2021 https://www.ema.europa.eu/endocuments/product-information/comirnaty-epar-product-information_en.pdf. Accesed 15 June 2021. „Neithergenotoxicity nor carcinogenicitystudieswereperformed. Thecomponents of thevaccine (lipids and mRNA) are notexpected to havegenotoxicpotential.“
23. Zhang L, Richards A, Barrasa MI, et al. Reverse-transcribed SARS-CoV-2 RNA canintegrateintothegenome of culturedhumancells and canbeexpressed in patient-derivedtissues. Proceedings of the National Academy of Sciences of the United States of America2021;118(21):e2105968118.
24. Doerfler W. AdenoviralVector DNA- and SARS-CoV-2 mRNA-Based Covid-19 Vaccines: PossibleIntegrationintotheHumanGenome – Are AdenoviralGenesExpressed in Vector-basedVaccines?. VirusResearch. 2021;302:198466.
25. Alegría-Torres JA, Baccarelli A, Bollati V. Epigenetics and lifestyle. Epigenomics. 2011;3(3):267-277. doi:10.2217/epi.11.22.
26. Santos-Rebouças CB, Pimentel MM. Implication of abnormalepigeneticpatternsforhumandiseases. EuropeanJournal of HumanGenetics : EJHG. 2007 Jan;15(1):10-7.
27. Burgio E, Piscitelli P, Colao A. EnvironmentalCarcinogenesis and TransgenerationalTransmission of Carcinogenic Risk: FromGenetics to Epigenetics. International Journal of EnvironmentalResearch and Public Health. 2018;15(8):1791.
28. Vaske OM, Bjork I, Salama SR, et al. Comparative Tumor RNA SequencingAnalysisforDifficult-to-TreatPediatric and YoungAdultPatientsWithCancer. JAMA NetworkOpen. 2019;2(10):e1913968.
29. Panditharatna E, Filbin MG. Thegrowing role of epigenetics in childhoodcancers. CurrentOpinion in Pediatrics. 2020 Feb;32(1):67-75.
30. Kubota Y, Uryu K, Ito T, et al. Integratedgenetic and epigeneticanalysisrevealedheterogeneity of acutelymphoblasticleukemia in Downsyndrome. CancerScience. 2019;110(10):3358–3367.
31. Tremblay MW, Jiang YH. DNA Methylation and Susceptibility to AutismSpectrumDisorder. AnnualReview of Medicine.2019;70:151–166.
32. Corley MJ, Vargas-Maya N, Pang APS, et al. EpigeneticDelay in theNeurodevelopmentalTrajectory of DNA MethylationStates in AutismSpectrumDisorders. Frontiers in Genetics. 2019;10:907.
33. Ellis SE, Gupta S, Moes A, et al. ExaggeratedCpHmethylation in theautism-affectedbrain. MolecularAutism. 2017;8:6. Published 2017 Feb 17.
34. Kichukova TM, Popov NT, Ivanov IS, Vachev TI. Profiling of circulatingserummicroRNAs in childrenwithautismspectrumdisorderusingstem-loopqRT-PCR assay. FoliaMedica (Plovdiv). 2017 Mar 1;59(1):43-52.
35. Lomniczi A, Wright H, Ojeda SR, et al. Epigeneticregulation of female puberty. Frontiers in Neuroendocrinology. 2015 Jan;36:90-107.
36. Toro CA, Aylwin CF, Lomniczi A. Hypothalamicepigeneticsdrivingfemale puberty. Journal of Neuroendocrinology. 2018 Jul;30(7):e12589
37. Vincent ZL, Farquhar CM, Mitchell MD, et al. Expression and regulation of DNA methyltransferases in humanendometrium.Fertility and Sterility. 2011 Mar 15;95(4):1522-5.e1.
38. Bommarito PA, Martin E, Fry RC. Effects of prenatalexposure to endocrinedisruptors and toxicmetals on thefetalepigenome. Epigenomics. 2017;9(3):333–350. 2018 Dec 1;47(6):1910-1937.
39. Leung AKL. TheWhereabouts of microRNAActions: Cytoplasm and Beyond. Trends in CellBiology. 2015 Oct;25(10):601-610.
40. Gedda MR, Babele PK, Zahra K, Madhukar P. EpigeneticAspects of EngineeredNanomaterials: IstheCollateralDamageInevitable? Front BioengBiotechnol. 2019 Sep 20;7:228.
41. Y. Zhao Q, Wu Y, Li, A. et al. In vivo translocation and toxicity of multi-walledcarbonnanotubes are regulated by microRNA. Nanoscale. 2014; 6: 4275-4284.
42. Yousef M, Goy G, Mitra R, et al. miRcorrNet: machinelearning-basedintegration of miRNA and mRNA expressionprofiles, combinedwith feature grouping and ranking. PeerJ.
2021;9:e11458.
43. Yao Y, Jiang C, Wang F, et al. IntegrativeAnalysis of miRNA and mRNA ExpressionProfilesAssociatedWithHumanAtrialAging. Frontiers in Physiology. 2019;10:1226.
44. Gross N, Kropp J, Khatib H. MicroRNASignaling in Embryo Development. Biology (Basel). 2017;6(3):34.
45. Selvaraj G, Kaliamurthi S, Peslherbe GH, Wei DQ. Are theAllergicReactions of COVID-19 VaccinesCaused by mRNA Constructs or Nanocarriers? ImmunologicalInsights. InterdiscipSci. 2021;13(2):344-347.
46. Sellaturay P, Nasser S, Islam S, Gurugama P, Ewan PW. Polyethyleneglycol (PEG) is a cause of anaphylaxis to the Pfizer/BioNTech mRNA COVID-19 vaccine. Clinical and experimentalallergy: journal of the British Society forAllergy and ClinicalImmunology. 2021;51(6):861-863. doi:10.1111/cea.13874.
47. Moghimi SM. AllergicReactions and Anaphylaxis to LNP-Based COVID-19 Vaccines. Moleculartherapy : thejournal of the American Society of GeneTherapy. 2021;29(3):898-900.
48. Santovito LS, Pinna G. Acutereduction of visualacuity and visualfieldafter Pfizer-BioNTech COVID-19 vaccine 2nd dose: a case report.Inflammationresearch : officialjournal of theEuropeanHistamineResearch Society. 2021;70(9):931-933.
49. Fowler N, MendezMartinez NR, Pallares BV, Maldonado RS. Acute-onsetcentralserousretinopathyafterimmunizationwith COVID-19 mRNA vaccine. American Journal of OphthalmologyCaseReports. 2021;23:101136.
50. TheJerusalem Post. MaayanJaffe-Hoffman.Pfizer COVID-19 vaccinelinked to rarecases of eyeinflammation– study. https://www.jpost.com/health-science/pfizer-covid-19-… Accessed 28 September 2021.
51. Fowler N, MendezMartinez NR, Pallares BV, Maldonado RS. Acute-onsetcentralserousretinopathyafterimmunizationwith COVID-19 mRNA vaccine. American Journal of OphthalmologyCaseReports. 2021;23:101136.
52. U.S. National Library of Medicine. MethylationEffects of COV-19 Infection and Vaccinations. Last Update Posted : June 30, 2021.https://clinicaltrials.gov/ct2/show/NCT04939155. Accessed 27 sep 2021.
53. WHO. COVID-19 adviceforthepublic: gettingvaccinated. Available at https://www.who.int/emergencies/diseases/novel-corona.. . Last update 14 July 2021. AccessedSeptember 28, 2021.
German panel giveslimitedapprovalfor COVID-19 shotforadolescents. Available at https://www.reuters.com/world/europe/german-panel-giv.. AccessedSeptember 28, 2021.
54. Children and adolescents. – informationaboutvaccinationagainst COVID-19. Public Health Agency of Sweden. https://www.folkhalsomyndigheten.se/thepublic-health-.. 20in%20August%202021. AccessedSeptember 28, 2021.
55. Children and adolescents. – information about vaccination against COVID-19. Public Health Agency of Sweden. https://www.folkhalsomyndigheten.se/thepublic-health-agency-of-sweden/communicable-disease-control/covid-19/vaccinationagainst-covid-19/children-and-adolescents–information-about-vaccination-against-covid19/#:~:text=In%20Sweden%2C%20vaccination%20against%20COVID,start%20sometime% 20in%20August%202021. Accessed September 28, 2021.
56. Plans to offer a vaccine to 16 and 17-year-olds. Available at https://www.regjeringen.no/en/aktuelt/plansto-offer-a-vaccine-to-16-and-17-year-olds/id2865629/ Accessed September 28, 2021.
V tomto článku sme sa venovali konkrétnej téme, ak máte chuť pokračovať v čítaní, určite si nenechajte ujsť aj ďalší článok Aby vám nenapršalo do nosa, pán Skrúcaný! , v ktorom sa venujeme inej oblasti a prinášame ďalšie zaujímavé pohľady a praktické informácie.